Reaktivita cykloalkanů
Řešená cvičení
Zatím zde nejsou žádné řešené příklady
Testy
-%
Reaktivita cykloakanů
Střední škola • 3 min
-%
Produkt bromace -%
Produkt hydrogenace -%
Podrobnosti o látce
Autor videa
Jan Blahut
Lektor chemie, fyziky, matematiky a českého jazyka.
Klíčová slova
Střední škola
Odhadovaná délka studia
0 h 10 min
Poznámka k videu
Cyklolkany jsou nasycené cyklické uhlovodíky. Jak už název napovídá, jedná se o zacyklené alkanu, tudíž jejich kruhy jsou složeny z jednotek \(-CH_2-\). Obecným vzorcem můžeme tuto skupinu charakterizovat jako \(C_nH_{2n}\) (někdy se lze setkat s označením \((CH_2)_n\)). Všímavý čtenář si jistě všimne faktu, že cykloalkan se oproti alkanu líší o dva vodíky kvůli zacyklení. Jako u alkanů se zde bavíme o molekulách obsahující opět pouze jednoduché vazby \(C-C\) a \(C-H\). Proto i reaktivita nebude nikterak odlišná, kromě nižších cykloalkanů.
Nižší cykloalkany (cyklopropan a cyklobutan) se od acyklických alkanů liší podstatně vyšší reaktivitou. Jejich nestabilita je dána úhlovým pnutím jejich kruhů. Zatímco u alkanů svírají vazby úhel přibližně 110°, u cyklopropanu to je 60° (trojúhelník = 3*60) a cyklobutanu 90° (čtverec = 4*90). Toto pnutí způsobuje vyšší energetickou náročnost systému. Reaktivnější jsou jednoduše proto, jelikož při reakci dochází k otevření kruhu, čímž se kruhové napětí uvolní a celkově se sníží energie systému (molekuly). Příklady rcí nižších cykloalkanů na následujícím schématu:
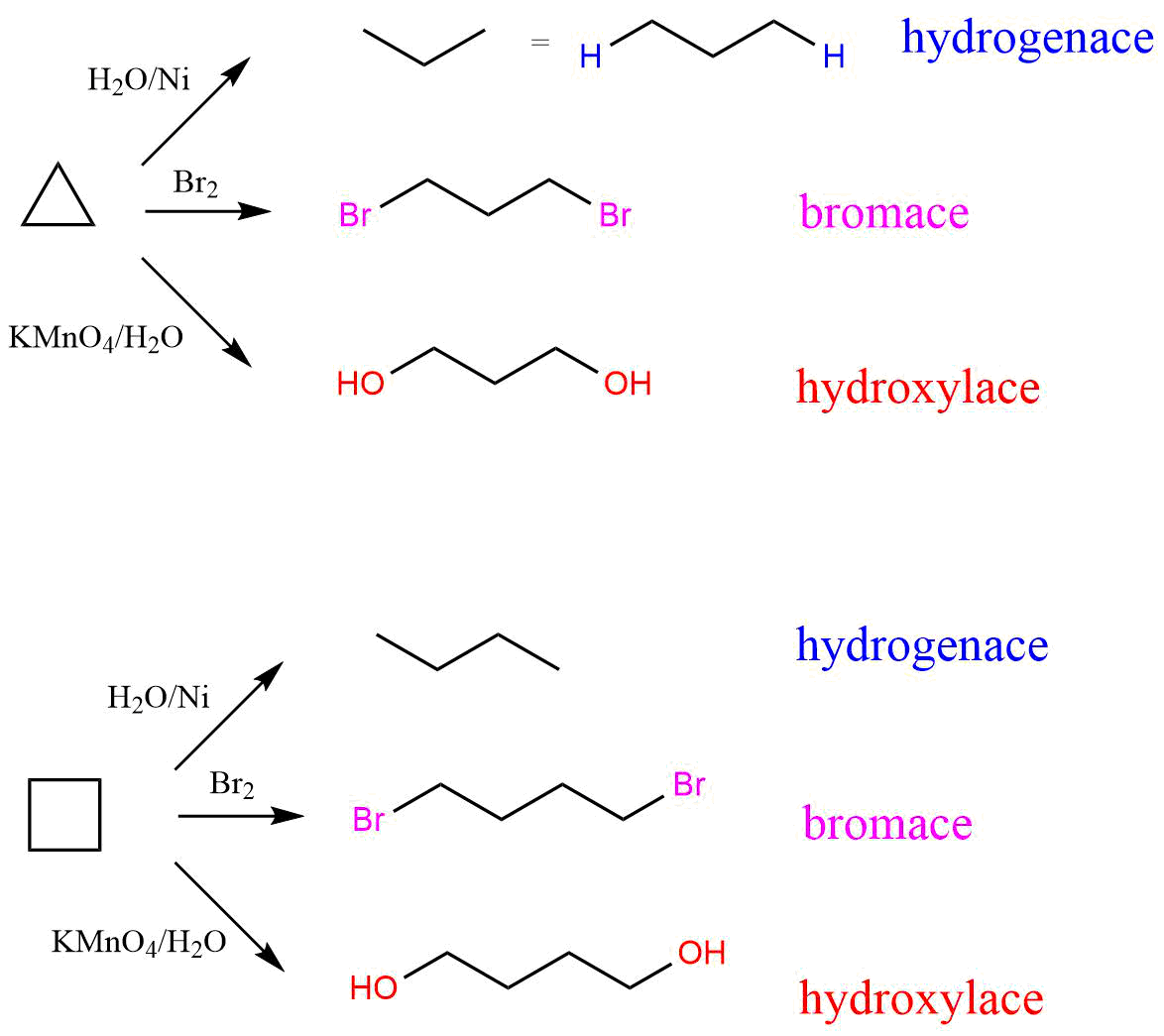
Obr. 1: Příklady rcí reaktivnějších nižších cykloalkanů (cyklopropan a cyklobutan)
Podobné rce podstupuje i cyklopentan. Pnutí vazeb u cyklopropanu není tak „vážné“, tudíž štěpení kruhu není tak snadné a je potřeba zvolit drastičtější reakční podmínky.
Vyšší cykloalkany mají větší stabilitu připodobitelnou k alkanům. Podstupují stejné rce jako alkany. Viz předešlé lekce.